 巴瑞氏食道
巴瑞氏食道
 巴瑞氏食道
巴瑞氏食道
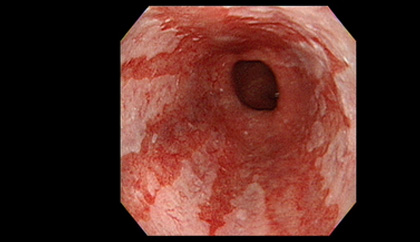
巴瑞氏食道(Barrett’s esophagus; BE)最早是在1950年時由倫敦的胸腔外科醫師諾曼巴瑞氏(Normann Barrett)醫師所提出,他從解剖的食道發現有些患者的食道潰瘍被柱狀黏膜所包圍,後來1953年艾力生與約翰史東(Allison and Johnstone)醫師發現下端的食道被柱狀細胞的胃黏膜所包覆,於是推測之前所謂巴瑞氏潰瘍可能是慢性胃食道逆流的產物,這個觀念逐漸為後人所接受並沿用至今。目前在美國估計大約有10-15%的胃食道逆流(GERD)患者有合併巴瑞氏食道,更重要的是巴瑞氏食道是個癌前病變,它可以演變成食道腺癌,這個癌症過去20年在美國已經增加了約5倍之多,並已超過食道鱗狀細胞癌,所以如何診斷並定期追蹤內視鏡檢查已成為一項重要的議題。
巴瑞氏食道從一開始的黏膜外觀發現到現在演變出許多不一樣的定義,目前較為大家所接受的定義是在2002年美國消化醫學會所定義的“a change in the esophageal epithelium of any length that can be recognized at endoscopy and is confirmed to have intestinal metaplasia by biopsy of the tubular esophagus and extends intestinal metaplasia of the cardia” 也就是說除了內視鏡要看到時到表皮的變化之外,還必須加上切片的病理報告顯示有腸化生的表現,最近在2006年又發表蒙特婁共識(Montreal definition),強調巨觀上內視鏡要觀察到舌頭樣且顏色似鮭魚的黏膜自胃食道交界處往食道突出,這樣的情況稱之為endoscopic suspected esophageal metaplasia (ESEM),若經由切片病理組織檢查證實有特定腸化生(specialized intestinal metaplasia)或胃化生(gastric metaplasia),才能得到巴瑞氏食道的診斷,但由於腸化生和未來的食道腺癌發生比較有關,所以有些研究只納入有腸化生的個案才稱為巴瑞氏食道。
在西方國家,巴瑞氏食道的盛行率在一般民眾約0.9-4.5%左右,但在有GERD的患者中則大約有6.3-13.6%,然而在東方國家則相對地較少(除了日本之外),盛行率約0.06-6.2%,盛行率的研究常因選取的研究族群不同、前瞻性與否、有無根據組織學來最後確認等因素而產生不同的結果,若根據最近在台灣以及韓國的大規模研究並採取目前較標準的診斷方式,巴瑞氏食道的盛行率在東方亞洲國家約0.85%,日本則因判定胃食道交界的方式與其他國家不同(採食道palisade vessel消失處),而超高的盛行率,但大都為長度不到一公分的巴瑞氏食道。一般而言罹患巴瑞氏食道的危險因子有年紀(愈大,大於50歲),性別(男:女約2:1),胃食道逆流的症狀(越嚴重或時間越久),食道疝脫,中廣型肥胖等,其他生活因子例如抽菸或喝酒在研究上較無確定的結論與巴瑞氏食道有關。然而值得注意的是仍約有40%的巴瑞氏食道患者是沒有上消化道症狀的。
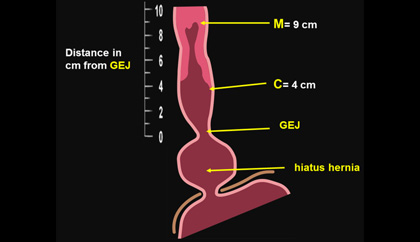
目前的診斷主要是靠內視鏡來尋找可疑的目標加上切片後來做組織學的確診,在內視鏡的診斷中傳統上根據其長度在胃食道交界(GEJ)以上大於或等於3公分者歸為long segment BE;小於3公分者則稱short segment BE,再加上內視鏡切片檢查可發現在long segment患者中約80%有intestinal metaplasia;但在short segment者中則僅有30%。因為此種分類太簡略所以International Working Group for the Classification of Oesophagitis (IWGCO)就訂定出新的分類,稱為布拉格分類(Prague C and M criteria),以巴瑞氏食道的高度:環狀病灶的最高長度 circumference (C)以及舌狀突出的最高長度 maximum (M),其中最重要的基準點是胃食道交界(GEJ)的位置,此點乃是C and M的起點,而在此分類的方法中也明確定義出如何決定GEJ的位置,以proximal margin of the gastric fold當內視鏡的指標點亦即胃皺摺的最高邊緣當GEJ的位置,如此一來便能輕鬆地量出C & M的長度,並能避開hiatal hernia的誤判干擾(Fig 1),
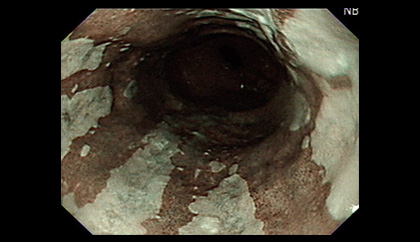
內視鏡切片採用西雅圖採樣步驟:每兩公分做四象限的隨機切片,而病理組織的診斷除了判定有無intestinal metaplasia以外,更重要的是要確定有無細胞異生(dysplasia),根據Vienna classification來判定是否有low grade or high grade dysplasia甚至於adenocarcinoma,因為此項組織學的分類判定會影響後續的追蹤以及治療方式,所以非常重要。有鑑於此,近年來在內視鏡光學的不斷進步下,很多學者試圖利用image-enhanced endoscopy (IEE)例如NBI, AFI等來尋找懷疑較嚴重的組織變化點,進行所謂的標靶切片(target biopsy),一般而言若欲針對dysplasia或adenocarcinoma座目標,AFI可以提高診斷的敏感度,而NBI則可以增加其特異度,也有新的內視鏡(tri-model system)合併傳統白光、AFI以及NBI試圖提高target biopsy的效果,雖有些好處,但仍有少數病灶仍靠隨機切片才發現,所以目前靠IEE做target biopsy仍是輔助隨機切片的互補功能,無法完全取代隨機切片的取樣。
巴瑞氏食道的治療首先要根據病理的報告來選擇,若是合併high grade dysplasia或早期的esophageal adenocarcinoma目前可以選擇電燒灼radiofrequency ablation(RFA) 或是內視鏡切除(EMR或ESD),其中RFA因為可以環狀大範圍消除dysplasia, early cancer甚至一般intestinal metaplasia,所以近年來在西方國家很盛行,效果相當良好,一般而言對dysplasia約有90%的根除率而intestinal metaplasia也有約80%的效果,根據最近的長期追蹤分析可知,約有13%會有intestinal metaplasia復發,約0.2%會被發現有食道腺癌,另外較嚴重的副作用是食道狹窄約佔5%。即使RFA效果相當良好,但根據成本效益分析僅有在high-grade dysplasia或早期食道腺癌才具效益。而EMR或ESD主要被應用於較局部的high grade dysplasia或黏膜層食道腺癌,不過目前大多是小規模的報告,其併發症是食道狹窄(10-30%),美國消化醫學會建議high-grade dysplasia可以使用RFA, photodynamic therapy或EMR來治療。
對於low-grade dysplsia或non-dysplasia的患者則建議進入內視鏡追蹤的計劃, 根據2008年American College of Gastroenterology建議(Table 1)。而藥物治療最常用的是氫離子幫浦阻斷劑(PPI),目前主要是用來控制GERD症狀,少數研究發現可以使BE由low-grade dysplasia回到non-dysplasia或是使BE的長度變短。

根據丹麥於2011年發表的大規模追蹤研究(11,028人)發現巴瑞氏食道的患者每年轉變成食道腺癌的發生率約0.12%,這個數值遠低於之前認為的0.5%,所以最近有在爭議是否要修訂內視鏡追蹤的時間間隔,然而一但產生食道腺癌之後,其預後相當不好,5年的存活率約僅有10%,所以只有在早期high-grade dysplasia或黏膜層腺癌先切入治療才有機會提高存活率。
義大醫院‧總機電話:07-615-0011‧07-952-0011 地址:82445高雄市燕巢區角宿里義大路1號
語音‧人工掛號專線:07-615-0900‧07-615-0911 週一至週五 07:30~16:30 週六 07:30~11:30
© Copyright 2014. "EDAGI" All rights reserved.